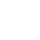
Zatrzymanie rozwoju zarodka na etapie kilku komórek (najczęściej w dniu 3., ale też w 2. lub 4., polega na tym, że zarodek dzieli się kilkukrotnie, jednak nie osiąga etapu moruli ani blastocysty. Po tych kilku podziałach nagle nie dzieje się nic – zarodek cały czas składa się z tej samej ilości blastomerów. Jego komórki żyją, ale przestają się dzielić.
Musimy zacząć od tego, że nie jest to zjawisko nietypowe. Wręcz przeciwnie – jest powszechne i występuje zarówno w warunkach laboratoryjnych jak i przy naturalnym zapłodnieniu.
W przypadku zapłodnienia metodą ICSI, prawidłowo zapłodni się średnio powyżej 65% komórek jajowych. Następnego dnia (dzień 2.) nastąpi podział (znów średnio) powyżej 95% z zapłodnionych komórek (w moim laboratorium 98,17% – dane z bieżącego roku 2022), czyli niemal wszystkich. Największa „strata” następuje właśnie około dnia 3., czyli w momencie, gdy zarodek składa się z kilku komórek (najlepiej 8, ale często jest to 4-12 blastomerów). Do etapu blastocysty dociera statystycznie około 40-70% z zapłodnionych komórek (w moim laboratorium 62,83% – dane z bieżącego roku 2022).
Co to oznacza? Znaczny odsetek zarodków zatrzymuje się w rozwoju właśnie na etapie kilku komórek. Około 40% pacjentów ma przynajmniej jeden zarodek, który przestał się dzielić w jednym cyklu leczenia. To całkiem powszechne zjawisko.
Poznajcie kilka przyczyn, które mogą leżeć u podstaw nieprawidłowego rozwoju zarodków.
Aktywacja genomu zarodka
Powyżej wspomniałam, że większość zarodków rozwija się do 3. dnia., zatem nie jest to żaden wyczyn dla zarodka. Bazując na materiale odżywczym w komórce, niemal każdy zarodek, jakby pchnięty magiczną siłą, będzie się rozwijał przez kilka pierwszych podziałów. Do trzeciego dnia genom, czyli materiał DNA zarodka jest „wyłączony”. Zarodek rozwija się dzięki temu, co znajduje się w komórce jajowej. W końcu żadna mama nie wyjeżdża w delegację zostawiając swoje dziecko bez jedzenia. Komórka jajowa to taka mini-wyprawka dla dziecka. W okolicach 3. dnia rozwoju (zarodek 4-8-komórkowy) następuje aktywacja genomu zarodka. To mniej więcej ten etap, kiedy mama zostaje w delegacji na dłużej i trzeba radzić sobie samemu. Sami wiecie, że nie każdemu wychodzi to najlepiej 😊 Jeśli aktywacja nie nastąpi – zarodek przestanie się rozwijać.
Matczyny RNA
Wspomniałam o „wyprawce od mamy”, która znajduje się w komórce jajowej i dzięki której zarodek może dzielić się i rozwijać aż do 3. dnia. W rzeczywistości są to transkrypty RNA, czyli przepisy, dzięki którym komórka może „ugotować” proste potrawy, czyli potrzebne do rozwoju białka. Komórka zawiera mnóstwo matczynego RNA dzięki któremu powstają białka zaangażowane w podziały zarodka, produkcję energii, reprogramowanie DNA oraz inne procesy. Do produkcji białek potrzebne są aminokwasy. Tych z kolei dostarcza zarodkowi embriolog, umieszczając go w specjalnym medium. Transkrypty są jak książka kucharska, a medium hodowlane jest jak lodówka, w której zarodek znajduje potrzebne składniki. Jeśli w zarodku zabraknie transkryptów, może to spowodować zahamowanie rozwoju zarodka. Podobnie, jeśli embriolog nie dostarczy zarodkowi odpowiedniego medium w odpowiedniej ilości, zarodek także może się zatrzymać w rozwoju. Pomimo, że aktualnie mamy bardzo dobrej jakości media hodowlane, cały czas w tej dziedzinie następuje duży rozwój, a naukowcy próbują udoskonalić pożywki zmieniając nieco ich skład.
Aneuploidie, czyli wady chromosomowe w zarodku
Według doniesień naukowych, po zbadaniu zarodków zatrzymanych w rozwoju wykazano, że aż 97,8% z nich było aneuploidalnych. Więcej możecie poczytać tutaj:
Wygląda na to, że wady genetyczne wpływają na rozwój zarodka, choć nie jest znany dokładny mechanizm. Wiadomo natomiast, że:
– więcej zarodków prawidłowych osiąga stadium blastocysty,
– zarodki zatrzymane w rozwoju są częściej aneuploidalne,
– w zarodkach, które przestały się dzielić wykazano wady więcej niż jednego chromosomu.
Oczywiście jeśli mówimy o wadach chromosomowych, nie sposób nie wspomnieć, że częściej występują one u kobiet po 35 roku życia. Według danych naukowych, u kobiet starszych większy odsetek zarodków zatrzymuje się na etapie 4-7 komórek. Więcej na ten temat w publikacji:
Frontiers | The Effect of Advanced Maternal Age on Embryo Morphokinetics (frontiersin.org)
Rola mitochondriów
U kobiet z wiekiem spada ilość mitochondriów w komórkach jajowych. Z lekcji biologii wiemy, że mitochondria to takie małe elektrownie w komórce, które dostarczają jej energii. Jeśli jest ich mniej lub ich funkcjonowanie zachodzi z mniejszą efektywnością, zarodek może mieć trudności z podziałem.
Wolne rodniki
ROS, czyli reaktywne formy tlenu indukują starzenie komórkowe. Mogą powodować uszkodzenia DNA, błon komórkowych, oksydację białek i skracanie telomerów. Zarodki hodowane w warunkach tlenu atmosferycznego wykazują wyższy poziom wolnych rodników i częściej zatrzymują się w rozwoju w porównaniu z hodowlą w 5% tlenie. Aktualnie większość laboratoriów zachowuje właściwe warunki hodowli zarodków, a więc powstawanie wolnych rodników jest ograniczone. Wciąż jednak funkcjonują laboratoria z inkubatorami „starego typu”, w których poziom tlenu wynosi 21%.
Matczyny kompleks podkorowy
Dość trudne pojęcie biologiczne – matczyny kompleks podkorowy (ang. subcortical maternal complex (SCMC)) to w rzeczywistości grupa białek, które znajdują się we wczesnym zarodku, współpracują ze sobą i promują przejście przez pierwsze podziały. Niestety nie wiemy o nim zbyt wiele. Wiemy, że jest zaangażowany:
– w formowanie i pozycjonowanie wrzeciona podziałowego w komórce (białka OOEP, NLRP5, TLE, KHDC3),
– w regulację translacji (FLOPED, MATER, TLE6, PADI6)
– w przemieszczanie mitochondriów do miejsc, gdzie potrzebna jest energia
– w epigenetyczne reprogramowanie (NLRP5, KHDC3L).
Kompleks jest więc niezwykle istotny i bez współpracy białek SCMC, zarodek przestanie się rozwijać.
Przykłady z publikacji naukowych:
– W przypadku mutacji genów kodujących białko PADI6 – u jednej pacjentki z 35 uzyskanych komórek jajowych 22 się zapłodniły i żaden zarodek nie rozwijał się dłużej niż do 3. dnia. Tutaj link do publikacji:
Mutations in PADI6 Cause Female Infertility Characterized by Early Embryonic Arrest – PMC (nih.gov)
– W przypadku mutacji genów kodujących białko TLE6 – u dwóch sióstr uzyskano 58 komórek jajowych, 3 się zapłodniły i zatrzymały się na etapie 1-4 komórek. Poniżej źródło naukowe:
Warto wiedzieć, że mutacje w genach kodujących białka SCMC są bardzo rzadkie.
Tutaj możecie poczytać więcej o kompleksie SCMC:
The subcortical maternal complex: multiple functions for one biological structure? – PMC (nih.gov)
Rola plemnika
Wolne rodniki
Jak wynika z badań na zwierzętach (myszy, małpy, bydło), wprowadzenie do komórki jajowej plemnika poddanego działaniu reaktywnych form tlenu (ROS), często prowadzi do zatrzymania rozwoju zarodka w momencie aktywacji genomu zarodka (czyli właśnie około 3. dnia). Należy wspomnieć, że reaktywne formy tlenu są niezbędne w fizjologicznych ilościach w przebiegu takich procesów jak kapacytacja czy reakcja akrosomowa. Jednak w przypadku podwyższenia ilości wolnych rodników, może dojść do uszkodzenia błony komórkowej i DNA plemnika. Stres oksydacyjny w plemnikach powoduje także zaburzenia demetylacji DNA w przedjądrzach męskich. O tych badaniach możecie poczytać więcej tutaj:
Ze względu na dużą rolę stresu oksydacyjnego, warto przed zabiegiem in vitro zbadać ROS w nasieniu oraz w przypadku wysokiego wyniku, zastosować 3-miesięczną terapię antyoksydacyjną lub selekcję plemników ZyMot.
Fragmentacja DNA plemników
Niższy odsetek blastocyst zaobserwowano w zabiegach in vitro, w których wykorzystano nasienie z nieprawidłową fragmentacją chromatyny (>30%). Potwierdza to na przykład poniższa publikacja:
Na efekty wpływa oczywiście w znaczącym stopniu wiek partnerki, gdyż jak wiadomo, niektóre uszkodzenia mogą zostać naprawione dzięki mechanizmom samonaprawy w zarodku. Ta samonaprawa przebiega skuteczniej u kobiet młodszych, przed 35 rokiem życia.
Warto w przypadku podwyższonej fragmentacji chromatyny zastosować metodę selekcji nasienia ZyMot lub MACS, aby plemniki wykorzystane do zapłodnienia in vitro były lepszej jakości.
Czynniki laboratoryjne
Głównym zadaniem embriologa jest stworzenie takich warunków do rozwoju zarodka, jakie panują w jajowodach i macicy, czyli w naturalnym środowisku. Jak już wspominałam wcześniej, zarodki powinny być hodowane w niższym stężeniu tlenu od stężenia atmosferycznego. Inkubatory zapewniają stałą temperaturę, a specjalne filtry HEPA zabezpieczają przed obecnością szkodliwych lotnych związków. Bez wdawania się w szczegóły: każdy element w laboratorium musi funkcjonować sprawnie, aby hodowla zarodków przebiegła bez zakłóceń.
Podsumowanie
- Część zarodków przestaje się rozwijać zanim osiągnie etapy moruli i blastocysty. Nie jest to zjawisko negatywne – to naturalna selekcja zarodków nieprawidłowych, wadliwych genetycznie. Problem zaczyna się wtedy, gdy odsetek blastocyst jest niski (poniżej 40%) lub gdy żaden zarodek nie osiąga etapu blastocysty. Musimy jednak zróżnicować sytuację, w której z 15 zapłodnionych komórek nie otrzymujemy żadnej blastocysty od sytuacji, w której z 2 zapłodnionych komórek nie otrzymujemy żadnej blastocysty. Statystycznie ryzyko zatrzymania w rozwoju dwóch zarodków jest dużo większe.
- Rola plemnika w zatrzymaniu rozwoju zarodka jest – moim zdaniem – przeceniana. Często słyszymy, że to plemnik odpowiada za to, że zarodki przestają się rozwijać po 3. dniu. Jak wynika z powyższego artykułu, rola komórki jajowej jest ogromna w porównaniu z rolą plemnika.
- Co jest najważniejsze? Komórka jajowa, plemnik czy wybór dobrego laboratorium? Każdy przypadek należy rozpatrywać indywidualnie, jednak najważniejsza zawsze jest komórka. Kiedy ona jest słabej jakości lub posiada wady genetyczne, ani najpiękniejszy plemnik, ani najlepszy embriolog już tego nie naprawią.
- Jak rozpoznać, gdzie leży problem, gdy odsetek uzyskanych blastocyst jest niski lub nie dochodzi do ich powstania?
– Jakości komórki jajowej (poza oceną jej morfologii pod mikroskopem), na ten moment nie da się dokładnie zbadać w sposób nieinwazyjny. Istnieją oczywiście mutacje pojedynczych genów, których badanie jest kosztowne i może nie przynieść żadnej odpowiedzi (głównie dlatego, że nie znamy wszystkich genów, które mogą wpływać na rozwój zarodka, mutacje te są także wyjątkowo rzadkie). Podobnie rzadko wykonywane są badania genetyczne komórki jajowej (a konkretnie ciałka kierunkowego). Jest to mało opłacalne i daje nam niewielką i niewystarczającą wiedzę – o wiele lepsze jest badanie blastocyst. Nie ma możliwości zbadania poziomu mitochondriów w oocytach, a jak wiemy, dysfunkcje mitochondriów powodują, że zarodek nie potrafi poradzić sobie z nadmiarem reaktywnych form tlenu. I tak koło się zamyka – wszystko jest powiązane. Wiele czynników musi współistnieć, aby zarodek rozwijał się prawidłowo. Znamy kilka potencjalnych mechanizmów prowadzących do zatrzymania rozwoju zarodka, ale wciąż trochę błądzimy po omacku. Nawet, jeśli przypuszczamy, że przyczyną jest komórka jajowa, nie zawsze mamy dostępne narzędzia, aby to udowodnić z całą pewnością.
– Jakość plemników możemy zbadać za pomocą prostych i szybkich testów (seminogram, ROS, chromatyna, HBA). Naukowcy cały czas prowadzą także badania w kierunku nowych możliwości diagnostycznych (choćby badania genetyczne, apoptozy, czy fosfolipazy C zeta). Te badania nie są jeszcze dostępne i póki co traktujemy je jako naukowe.
– Najłatwiej zbadać skuteczność laboratorium. Mierzy się ją poprzez KPI (key point indicators), czyli specjalne wskaźniki, które mówią nam, czy dana procedura daje pożądane efekty. Jak to działa? Przykładowo, powinniśmy średnio uzyskać powyżej 40% blastocyst, czyli tzw. „competency value”, co oznacza, że zarodki mają optymalne warunki do rozwoju, jak w hotelu 3-gwiazdkowym. Natomiast laboratorium uzyskujące powyżej 60% blastocyst przekroczyło tzw. „benchmark value”, czyli zarodkom jest w nim tak dobrze, jak w 5-gwiazdkowym hotelu 😊Takich KPI jest więcej i dotyczą właściwie każdego etapu od punkcji aż po transfer. Oczywiście KPI nie liczymy u pojedynczych pacjentów, tylko w całej grupie np. na przestrzeni 1 miesiąca. Jeśli w danym miesiącu skuteczność utrzymuje się na tym samym poziomie, oznacza to prawidłowe funkcjonowanie laboratorium. Jeśli u pojedynczej pary nie uzyskamy żadnej blastocysty, mamy pewność, że problem leży po stronie komórek jajowych lub plemników. Jeśli natomiast u kilku par z rzędu nie uzyskamy żadnej blastocysty – problem mamy w samym laboratorium.
– Pomocnym narzędziem w zdiagnozowaniu problemu zatrzymania podziałów zarodka może być inkubator time lapse. Dzięki stałemu podglądowi rozwoju zarodków, embriolog wychwytuje pojawiające się na różnych etapach dodatkowe zmiany. Direct cleavage, reverse cleavage, multinukleacja – zjawiska związane z błędnymi podziałami komórek sugerują, że z zarodkiem coś jest nie tak już w dniu 1. lub 2., mimo tego, że zarodek dalej się dzieli i rozwija. Nawet, jeśli zatrzyma się w dniu 3., to ważniejsze jest to, że wcześniej też nie rozwijał się dobrze, a przyczyna może być zarówno męska jak i żeńska (ale jednak częściej żeńska). Także fragmentacja stanowi nieprawidłowy element rozwoju zarodka i uważa się, że wynika raczej z nieprawidłowości w oocycie lub w przebiegu mitoz (podziałów komórkowych). Zbyt wolne lub zbyt szybkie tempo podziałów sugeruje nieprawidłowości genetyczne, biochemiczne lub rozwojowe, które mogą wynikać zarówno z przyczyny męskiej jak i żeńskiej (ale jednak częściej z żeńskiej).